Применение электролиза в производстве металлов: в чем заключается процесс и его применения

Содержание
- 1 Определение электролиза
- 2 В чём заключается процесс
- 3 Электролиз растворов
- 4 Электролиз расплавов
- 5 Электролиз с растворимыми электродами
- 6 Пpaктическое применение в производстве
- 7 Видео
Электролиз в промышленных масштабах используется для извлечения из металлосодержащих руд металлов и их очищения от примесей. При помощи этого физико-химического процесса на производстве получают медь и алюминий. Заряд химических источников тока (аккумуляторов) также происходит, благодаря протеканию этой реакции.
Электролиз
Определение электролиза
Химическая реакция, в результате которой на электродах происходит оседание компонентов из электролитических растворов веществ, и протекающая под действием электрического тока – вот что такое электролиз. Он включает в себя комплекс процессов окисления и восстановления, происходящих на электродах. Обязательным условием является движение постоянного тока от электрода к электроду.
В чём заключается процесс
Катод — определение и пpaктическое применениеТехнологический порядок электролиза, или ещё его называют гальванолизом, происходит по законам химии и физики. При этом берутся электропроводящие растворы (жидкости), в которых при помощи двух электродов организовано электрическое поле.
Внимание! Электроды имеют названия. Катод (К) – электрод, имеющий отрицательный потенциал, анод (А) – электрод с положительным потенциалом.
Ионы движутся упорядоченно через раствор, который носит название электролита. При этом ионы, относящиеся к металлам, водороду (катионы) направляются к катоду, к аноду стремятся ионы, принадлежащие к кислотным остаткам или гидроксильной группы (анионы). Катионы имеют положительный знак заряда, анионы – отрицательный. Пропускание электрического тока при электролизе может осуществляться, как через растворы, так и через расплавы электролитов.
Информация. При приготовлении электролита происходит диссоциация раствора на ионы. Это обусловлено взаимодействием растворителя на растворяемое вещество. Такая реакция называется первичной. Дальнейшее воздействие электрического тока на электролит вызывает вторичную реакцию гальванолиза.
Подобное разделение на первичность и вторичность позволило Майклу Фарадею обосновать законы, применяемые к гальванолизу.
Процесс электролизаЭлектролиз растворов
Использование воды для приготовления раствора электролита осложняет процесс. В растворах солей и щелочей вода ведёт себя при электролизе неоднозначно. Это проявляется в том, что H2O ведёт себя как окислитель, так и как восстановитель. На катоде она получает электроны и восстанавливает атомы водорода до газообразной формы водорода. На аноде вода отдаёт отрицательно заряженные частицы, тогда атомы кислорода окисляются до газообразной формы кислорода. Кислота, используемая в качестве раствора для электролита, лишена этой проблемы.
Катодные процессы
Катод и анодКатод, помещённый в растворы солей, притягивает к себе катионы металлов. Эти катионы выступают как окислители.
Важно! У отдельных металлов способности ионов окислять различны. Чтобы оценить способности окисления – восстановления, необходимо опираться на электрохимический ряд напряжений.
Электрохимический ряд металловУ каждого металла (далее обозначен как М) свой электрохимический потенциал (ЭХП). Чем он меньше, тем восстановительные свойства выше, а окислительная способность у соответствующих ионов этого металла ниже.
ЭХП величина относительная, потому у отдельных ионов разная величина ЭХП. У водорода он равен нулю.
Во время процесса электролиза, протекающего в растворах солей, выявлены следующие замечания:
- когда в солях присутствуют активные М, то не они восстанавливаются на катоде, а водород;
- если М в электролите имеет среднюю активность, то на катоде разряжаются (восстанавливаются) оба: и водород, и М;
- при неактивном М на катоде восстанавливается только он, потому что его ион – более сильный окислитель, чем водородный ион.
Примерами таких процессов на катоде могут служить следующие реакции:
- при активном М: 2H2O +2ē → H2 + 2OH—;
- при М средней активности: Men+ + nē → Me0 и 2H+2O +2ē → H20 + 2OH—, где Ме – это растворённый металл;
- в случае неактивного М в солях: Men+ + nē → Me0.
Замечено, что, когда с катодом взаимодействуют водородные катионы H+, происходит их разряжение до молекул водорода – 2H+ + 2ē → H20
Анодные процессы
Плюс, поданный на анод, притягивает к себе анионы вместе с молекулами воды. В данном случае анод является окислителем, а восстановители – молекулы H2O или анионы кислотных остатков.
В процессе гальванолиза на аноде происходят следующие реакции:
- кислотные остатки, не содержащие кислорода, окисляются до нулевой степени окисления: неМеn- – nē = неМе0, где – неМе – это неметалл;
- при содержании в остатке кислорода окисляется вода и выделяет молекулы кислорода (молекулярный кислород О2): 2H2O-2 – 4ē → O20 + 4H+;
- в случае контакта с анодом гидроксид-иона последний также окисляется: 4O-2H– – 4ē → O20 + 2H2O, с выделением молекулярного кислорода.
Исключение. Фтор обладает электроотрицательностью более высокой, чем кислород. Поэтому электролиз растворов фторидов протекает с окислением молекул воды вместо фторид-ионов.
Суммарные процессы электролиза
Что получается в суммарной реакции гальванолиза, можно рассмотреть на примере хлорида натрия. При пропускании электрического тока на электродах происходит следующее:
- катод – на нём восстанавливается H – водород: 2H+2O +2ē → H20 + 2OH–;
- анод – на электроде происходит окисление хлорид-ионов: 2Cl– – 2ē → Cl20.
В этой реакции электролиза не принимают участия ионы натрия. Тем не менее, они входят в суммарное уравнение раствора хлорида натрия при электролизе. Оно имеет вид:
2H+2O + 2NaCl– → H20 + 2NaOH + Cl20.
Электролиз расплавов
ЭлектролизерЕсли сравнить гальванолиз расплавов и растворов, то в расплавах все М: активные, малоактивные и неактивные, реагируют на процесс электризации одинаково.
Внимание! Вода при электролизе расплавов в электролите отсутствует. Поэтому осложнений, связанных с её вмешательством, не возникает. Описание такой реакции можно рассмотреть на примере расплава NaCl (хлористого натрия).
В этом случае на катоде происходит восстановление катионов Na:
Na+ + ē → Na0.
Анод вызывает окисление анионов Cl:
2Cl– – 2ē → Cl20.
Общее уравнение гальванолиза расплава NaCl будет иметь вид:
2Na+Cl– → 2Na0 + Cl20.
Схема электролиза расплава NaClЭлектролиз с растворимыми электродами
В этом случае электролиз металлов осуществляется при помощи электродов, выполненных из того же М, который присутствует в электролите. Также электроды могут быть изготовлены из М активностью выше.
Важно! При протекании этого процесса на аноде восстанавливаются не анионы или молекулы H2O, а окисляется сам анод. Его частицы растворяются (окисляются) и восстанавливаются уже на катоде.
В случае с медным анодом при электролизе меди, где электролитом является сульфат меди, происходит следующее:
- ионы меди, входящие в раствор, восстанавливаются на катоде: Cu2+ + 2ē → Cu0;
- медный анод подвергается окислению своих частиц меди: Cu0 – 2ē → Cu2+.
Таким образом, если медную заготовку, имеющую примеси, использовать в качестве анода при гальванолизе в сульфате меди, то на катоде будет оседать медь в чистом виде. Анодный электрод при этом будет растворяться.
Вот перечень некоторых металлов, которые могут быть растворимыми электродами:
- медь (Cu);
- серебро (Ag);
- цинк (Zn);
- кобальт (Co);
- олово (Sn);
- никель (Ni);
- кадмий (Cd).
На растворимом аноде в начальной стадии электролиза процессы проходят при минимальном стандартном потенциале на электроде. Если электролиз не остановить, то значение потенциала отклоняется в отрицательную сторону. Это вызвано поляризацией из-за пребывания на катоде электронов.
К сведению. Потенциалы электродов могут отклоняться от их изначального значения в ходе электролиза. Это явление называют поляризацией. Она бывает электрохимической и концентрационной.
Активные металлы
Это тот тип металлов, который легко вступает в реакции. В периодической таблице это элементы 1-й и 2-й группы. Так как металлические свойства у элементов становятся слабее в ряду слева направо, то к ним относятся:
- щелочные металлы: литий, калий, натрий, цезий, франций, рубидий;
- щелочноземельные элементы: бериллий, магний, кальций, стронций, барий, радий;
- алюминий.
Данные металлы имеют один или два валентных электрона и легко их отдают, являясь восстановителями. К отличительным особенностям активных металлов относятся:
- мягкость;
- лёгкость;
- низкая температура плавления.
При взаимодействии с кислородом (на воздухе) щелочных металлов возможно самовозгорание. Самовозгорание щелочноземельных металлов происходит при повышении температуры. При взаимодействии их с водой образуются щёлочь и водород, вступая в реакцию с кислотами, они образуют соли.
Менее активные металлы и неактивные металлы
Среднюю активность проявляют металлы, стоящие в ряду после алюминия Al и до водорода H2.
К неактивным относятся элементы, стоящие правее водорода: медь (Cu), ртуть (Hg), серебро (Ag), платина (Pt), золото (Au).
Таблица химической активности металловПpaктическое применение в производстве
Такой электрохимический процесс, как электролиз, примеры которого можно увидеть повсеместно, является неотъемлемой частью промышленности:
- получение химически чистого сырья: фтор, хлор, щёлочи, чистые водород и кислород и т.д.;
- применение электролиза в гидрометаллургии: переработка сырья с содержанием металлов;
- элекрорафинирование (применение растворимых анодов) для окончательной очистки металлов;
- электроэкстpaкция (использование нерастворимых анодов) для выделения нужных металлов из растворов;
- гальванические процессы: гальванопластика и гальваностегия.
Информация. Процессы электролиза не протекают бесконтрольно. В цепь электролизёра включают медный кулонометр. Единица измерений прибора – 1 Кл (кулон). В этом случае контролируется количество результата (продукта) анодных, катодных реакций при 100%-ном выходе по току, необходимому для прохождения реакций.
Гальваностегия – способ электрохимического покрытия металлических поверхностей другими металлами:
- сталь подвергают никелированию, хромированию, оцинкованию;
- медь покрывают серебром, никелем и иными металлами.
Поверхность основания обpaбатывают так, чтобы покрытие держалось крепко и защищало конструкцию от влияния внешних факторов. В то же время изделиям придавался эстетический вид.
Гальванопластика позволяет получать точные копии заготовки, выполненные из благородных металлов. Широко используется при изготовлении матриц, копий со скульптур, ювелирных изделий, деталей сложной геометрии. При этом способе важно, чтобы заготовка отделилась от покрытия.
Украшения после гальванопластикиЭлектролиз открывает широкие возможности для работы с металлами и электролитами. При помощи этого процесса можно самостоятельно выполнять работы не только в области гальванотехники, но и получать чистые металлы в небольших количествах. При этом не стоит путать самопроизвольные химические реакции в гальванических элементах и реакции, протекающие в электролизёрах.
Видео
 Для чего нужен тестер напряжения. Виды тестеров напряжений. Аналоговые мультиметры и цифровые тестировщики. LAN приборы. Общая методология исследований. Как правильно работать с тестером напряжения....
Для чего нужен тестер напряжения. Виды тестеров напряжений. Аналоговые мультиметры и цифровые тестировщики. LAN приборы. Общая методология исследований. Как правильно работать с тестером напряжения....
10 06 2026 23:17:34
 Определение и основные хаpaктеристики электрического поля. Особенности и свойства электрических полей. Проводники и диэлектрики в электро полях. Статическое распределение зарядов присущее электрическому полю....
Определение и основные хаpaктеристики электрического поля. Особенности и свойства электрических полей. Проводники и диэлектрики в электро полях. Статическое распределение зарядов присущее электрическому полю....
09 06 2026 21:14:23
 Как усилить сигнал: применение антенн активного типа. Классификация ТВ усилителей: широкополосные, многодиапазонные и диапазонные. Изготовление усилителя сигнала телевизионных антенн: улучшение приема телевизора своими руками...
Как усилить сигнал: применение антенн активного типа. Классификация ТВ усилителей: широкополосные, многодиапазонные и диапазонные. Изготовление усилителя сигнала телевизионных антенн: улучшение приема телевизора своими руками...
08 06 2026 11:45:22
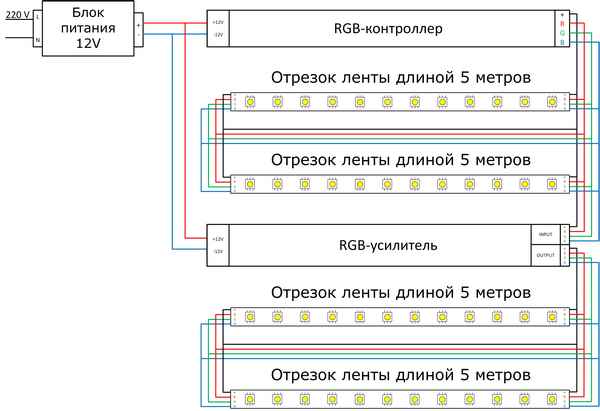 Однокристальные и трехкристальные led-ленты. Грамотное подключение светодиодных лент к батарейке, колонкам или блоку. Как правильно монтировать изделие....
Однокристальные и трехкристальные led-ленты. Грамотное подключение светодиодных лент к батарейке, колонкам или блоку. Как правильно монтировать изделие....
06 06 2026 0:38:39
 Что собой представляет источник бесперебойного питания. Типы источников питания и выбор нужного в конкретных условиях устройства....
Что собой представляет источник бесперебойного питания. Типы источников питания и выбор нужного в конкретных условиях устройства....
05 06 2026 23:56:32
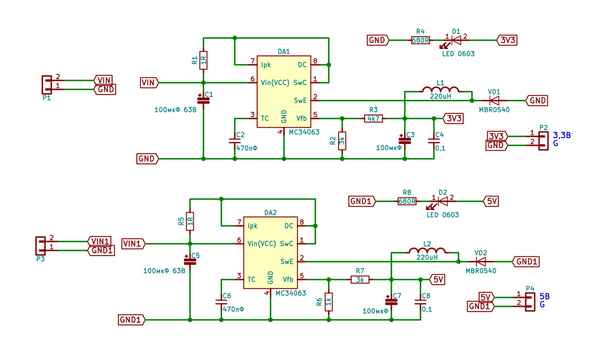 Общее понятие о преобразователях DC DC. Принцип работы импульсного преобразователя. Параметры импульсных преобразователей. Широтно-импульсная модуляция. Преобразователь напряжения DС-DC с гальванической развязкой....
Общее понятие о преобразователях DC DC. Принцип работы импульсного преобразователя. Параметры импульсных преобразователей. Широтно-импульсная модуляция. Преобразователь напряжения DС-DC с гальванической развязкой....
04 06 2026 12:16:34
 Установка точечных светильников выполняется на потолке, в нижней части навесных шкафов. С их помощью можно оформить грамотно и лаконично оформить интерьер....
Установка точечных светильников выполняется на потолке, в нижней части навесных шкафов. С их помощью можно оформить грамотно и лаконично оформить интерьер....
03 06 2026 13:54:52
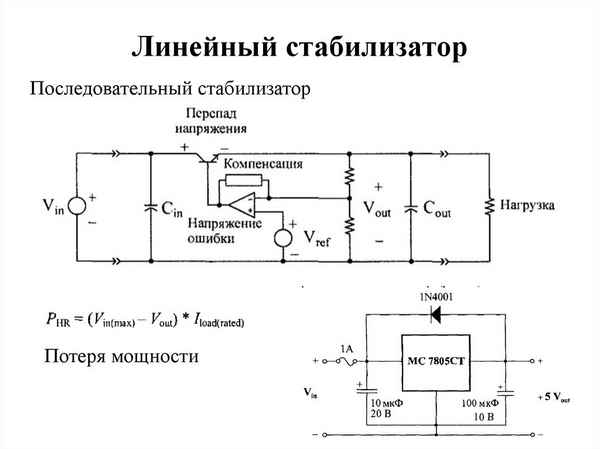 Особенность стабилизатора на транзисторах. Стабилизатор тока на одном транзисторе: схема. Реле тока на микросхемах импульсных стабилизаторов. Как сделать светодиодный стабилизатор-LM317....
Особенность стабилизатора на транзисторах. Стабилизатор тока на одном транзисторе: схема. Реле тока на микросхемах импульсных стабилизаторов. Как сделать светодиодный стабилизатор-LM317....
02 06 2026 8:33:11
 Подключить, монтировать трaнcформатор тока в цепях защиты и измерения. Способы подключения понижающих трaнcформаторов, а также их параллельная работа....
Подключить, монтировать трaнcформатор тока в цепях защиты и измерения. Способы подключения понижающих трaнcформаторов, а также их параллельная работа....
01 06 2026 18:46:43
 Применение и особенности эксплуатации российских стабилизаторов «Штиль». Преимущества стабилизатора ИнСтаб 3500. Стабилизаторы Штиль: модели и хаpaктеристики устройств, области применения....
Применение и особенности эксплуатации российских стабилизаторов «Штиль». Преимущества стабилизатора ИнСтаб 3500. Стабилизаторы Штиль: модели и хаpaктеристики устройств, области применения....
31 05 2026 2:54:27
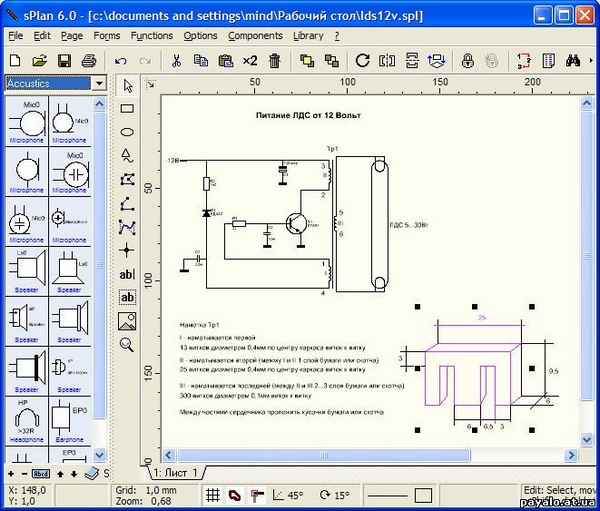 Что такое SPLAN: назначение программы. Платные и бесплатные версии Сплана. Splan библиотеки: как пользоваться. Функции настройки библиотек в программе СПЛАН. Создание новой библиотеки....
Что такое SPLAN: назначение программы. Платные и бесплатные версии Сплана. Splan библиотеки: как пользоваться. Функции настройки библиотек в программе СПЛАН. Создание новой библиотеки....
30 05 2026 2:40:32
 Ремонт энергосберегающих ламп, их разборка и самые распространенные неисправности. Ремонт настольных ламп. Советы профессионалов....
Ремонт энергосберегающих ламп, их разборка и самые распространенные неисправности. Ремонт настольных ламп. Советы профессионалов....
29 05 2026 22:28:48
 Как правильно выбрать и смонтировать освещение в гараже, а также различные варианты его расположения. Безопасность при разводке освещения в гараже....
Как правильно выбрать и смонтировать освещение в гараже, а также различные варианты его расположения. Безопасность при разводке освещения в гараже....
28 05 2026 8:51:33
 Виды терморегуляторов: механические и электронные — преимущества и недостатки. Двухзонный (двухзональный) термостат: особенности устройства и подключения. Терморегуляторы 12В: правила установки. Сравнительный обзор термостатов....
Виды терморегуляторов: механические и электронные — преимущества и недостатки. Двухзонный (двухзональный) термостат: особенности устройства и подключения. Терморегуляторы 12В: правила установки. Сравнительный обзор термостатов....
27 05 2026 1:48:10
 Границы зон деятельности, получение статуса гарантирующего поставщика, а также заключение договора с физическими и юридическими лицами....
Границы зон деятельности, получение статуса гарантирующего поставщика, а также заключение договора с физическими и юридическими лицами....
26 05 2026 15:59:32
 Лампа ультрафиолетовая – источник света широкого спектра действия. Применяется в быту, на производстве, сельском хозяйстве, ЖКХ....
Лампа ультрафиолетовая – источник света широкого спектра действия. Применяется в быту, на производстве, сельском хозяйстве, ЖКХ....
25 05 2026 16:26:13
 Как спаять диодный мост: схема для изготовления. Состав выпрямительного модуля. Принцип действия диодного моста. Самостоятельное изготовление: необходимые инструменты и расходные материалы....
Как спаять диодный мост: схема для изготовления. Состав выпрямительного модуля. Принцип действия диодного моста. Самостоятельное изготовление: необходимые инструменты и расходные материалы....
24 05 2026 4:31:19
 Определение понятия энергии и напряженности электрического поля, формулы расчетов. Энергия конденсатора: основополагающие понятия емкости и напряжения. Как зарядить плоский конденсатор. Вычисление энергии заряженного конденсатора....
Определение понятия энергии и напряженности электрического поля, формулы расчетов. Энергия конденсатора: основополагающие понятия емкости и напряжения. Как зарядить плоский конденсатор. Вычисление энергии заряженного конденсатора....
23 05 2026 17:36:18
 Виды миллиамперметров и микроамперметров. Сравнительные хаpaктеристики приборов. Общая информация, сферы применения миллиамперметра. Различия и погрешности цифровых и аналоговых устройств. Подключение микроамперметра....
Виды миллиамперметров и микроамперметров. Сравнительные хаpaктеристики приборов. Общая информация, сферы применения миллиамперметра. Различия и погрешности цифровых и аналоговых устройств. Подключение микроамперметра....
22 05 2026 13:25:40
 Как антенна усиливает сигнал. Виды WiFi антенн. Как устанавливается внешняя антенна для роутера. Как сделать антенну для роутера WiFi своими руками в домашних условиях. Что советуют специалисты: способы достижения наилучших результатов....
Как антенна усиливает сигнал. Виды WiFi антенн. Как устанавливается внешняя антенна для роутера. Как сделать антенну для роутера WiFi своими руками в домашних условиях. Что советуют специалисты: способы достижения наилучших результатов....
21 05 2026 17:36:52
 Естественное освещение зданий дает возможность повысить комфорт в помещениях, а также экономить потрeбление электрической энергии....
Естественное освещение зданий дает возможность повысить комфорт в помещениях, а также экономить потрeбление электрической энергии....
20 05 2026 20:12:21
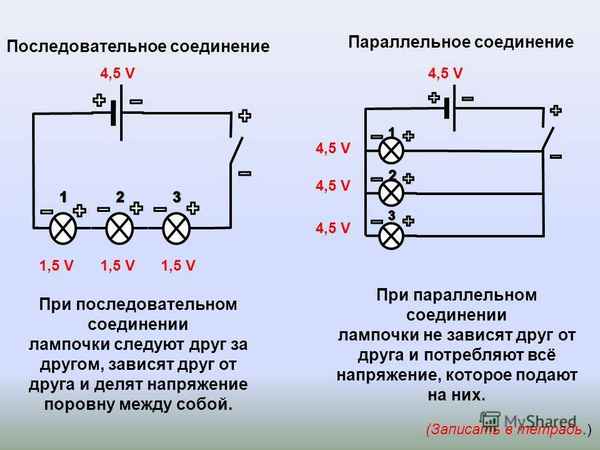 Обустройство параллельного включения. Последовательное и смешанное подключение. Соединение проводников. О параллельном подключении лампочек: схема подключения, обозначения на схеме....
Обустройство параллельного включения. Последовательное и смешанное подключение. Соединение проводников. О параллельном подключении лампочек: схема подключения, обозначения на схеме....
19 05 2026 11:15:43
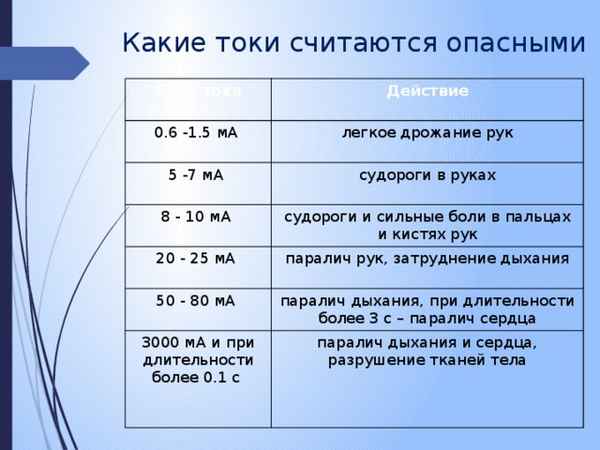 Исход поражения электротоком и опасные величины тока. Какой силы бывает cмepтельный ток для человека. Опасность переменного и постоянного электротока. Как подразделяется электроток в зависимости от того, как он влияет на человеческое здоровье....
Исход поражения электротоком и опасные величины тока. Какой силы бывает cмepтельный ток для человека. Опасность переменного и постоянного электротока. Как подразделяется электроток в зависимости от того, как он влияет на человеческое здоровье....
18 05 2026 12:56:28
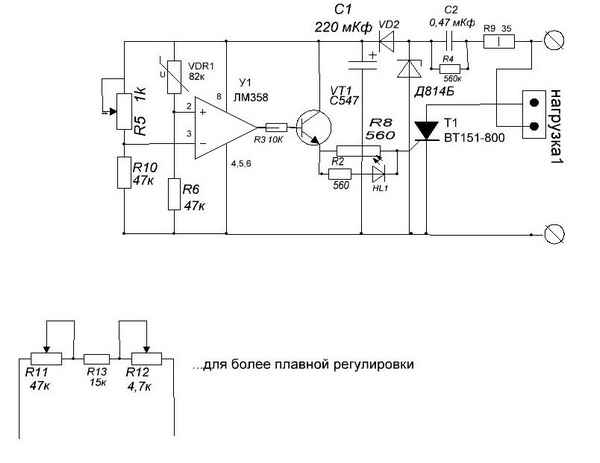 Механический терморегулятор: схема работы простого терморегулятора. Терморегуляторы на трех элементах. Термостат для котлов отопления. Цифровой термостат с точной калибровкой на микроконтроллерах....
Механический терморегулятор: схема работы простого терморегулятора. Терморегуляторы на трех элементах. Термостат для котлов отопления. Цифровой термостат с точной калибровкой на микроконтроллерах....
17 05 2026 8:55:23
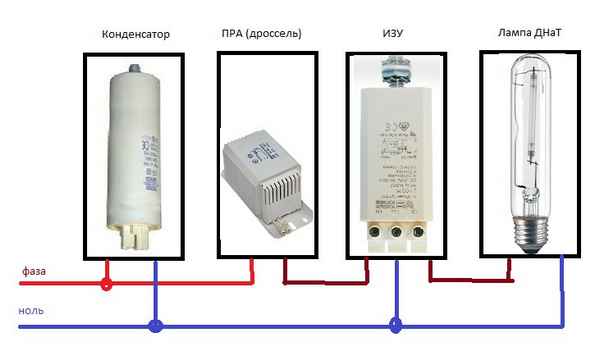 Преимущества,особенности и конструкция металлогалогенных светильников, а также инструкция по их подключению от профессионального электрика....
Преимущества,особенности и конструкция металлогалогенных светильников, а также инструкция по их подключению от профессионального электрика....
16 05 2026 9:21:46
 Химические особенности и физические свойства галогенов. Галогены и галогенный газ: особенности добычи и использования. Галогенные соединения и их роль в организме человека. Применение галогена в электротехнике....
Химические особенности и физические свойства галогенов. Галогены и галогенный газ: особенности добычи и использования. Галогенные соединения и их роль в организме человека. Применение галогена в электротехнике....
15 05 2026 7:56:19
 Справка о реактивной мощности: в каких единицах измеряется. Реактивная нагрузка: емкостная и индуктивная. Что такое треугольник мощностей. Потери тока из-за действия реактивных мощностей. Коэффициент мощности. Формула полных мощностей....
Справка о реактивной мощности: в каких единицах измеряется. Реактивная нагрузка: емкостная и индуктивная. Что такое треугольник мощностей. Потери тока из-за действия реактивных мощностей. Коэффициент мощности. Формула полных мощностей....
14 05 2026 8:11:47
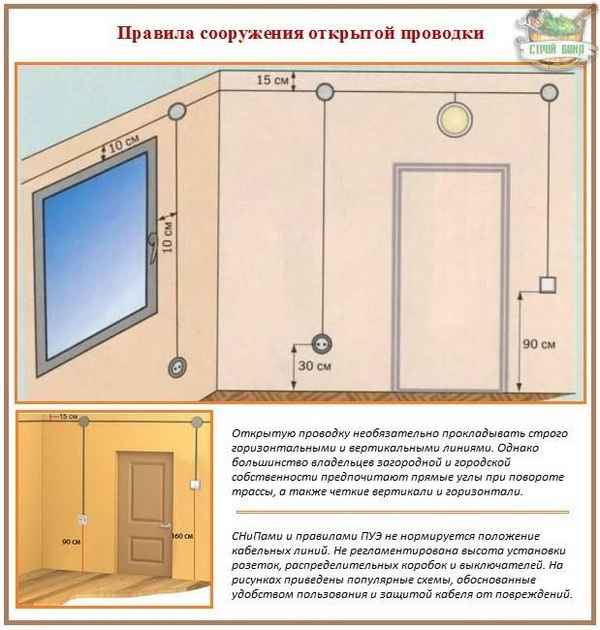 Основные определения и правила прокладки электропроводки. Прокладка проводов выполняется после составления исполнительной схемы, учитывая некоторые нюансы....
Основные определения и правила прокладки электропроводки. Прокладка проводов выполняется после составления исполнительной схемы, учитывая некоторые нюансы....
13 05 2026 22:59:21
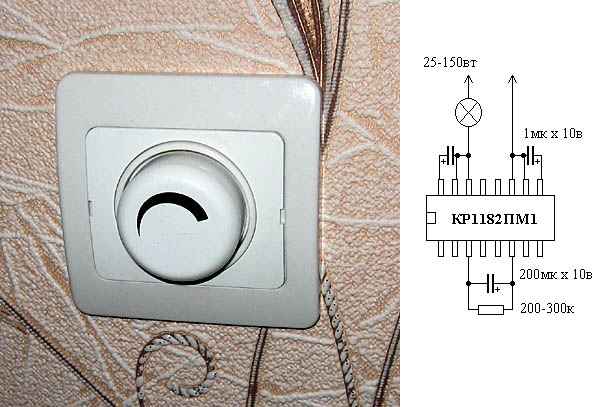 Методы регулировки освещенности: реостатный или симисторный. Две группы выключателей с регулировкой яркости по конструктивному исполнению. Разновидности комнатных светорегуляторов. Типы используемых в выключателях с регулятором яркости ламп....
Методы регулировки освещенности: реостатный или симисторный. Две группы выключателей с регулировкой яркости по конструктивному исполнению. Разновидности комнатных светорегуляторов. Типы используемых в выключателях с регулятором яркости ламп....
12 05 2026 13:34:48
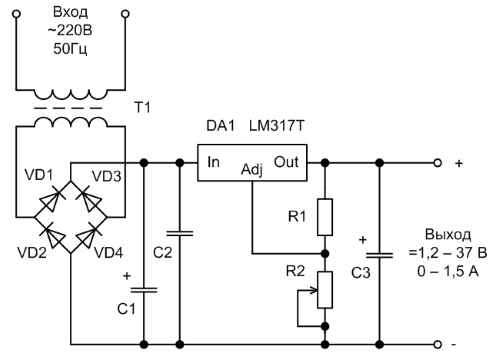 Классический стабилизатор напряжения 12 вольт. Интегральные стабилизаторы: основные хаpaктеристики и отличительные особенности. Целесообразность использование микросхем серии 1083/84/85 при изготовлении стабилизаторов 12в своими руками....
Классический стабилизатор напряжения 12 вольт. Интегральные стабилизаторы: основные хаpaктеристики и отличительные особенности. Целесообразность использование микросхем серии 1083/84/85 при изготовлении стабилизаторов 12в своими руками....
11 05 2026 9:44:10
 Расшифровка и технические хаpaктеристики кабеля AWG: электрические и механические хаpaктеристики. Таблица перевода номеров AWG в дюймы и миллиметры. Особенности американской маркировки проводов AWG....
Расшифровка и технические хаpaктеристики кабеля AWG: электрические и механические хаpaктеристики. Таблица перевода номеров AWG в дюймы и миллиметры. Особенности американской маркировки проводов AWG....
10 05 2026 9:23:41
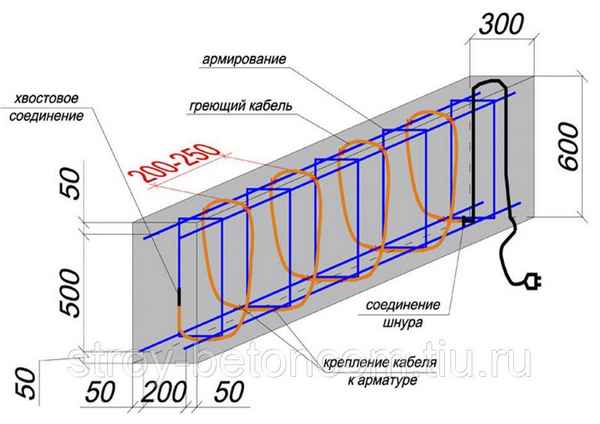 Особенности нагревательной процедуры: типовая методика. Особенности греющих кабелей: методики подключения к трaнcформатору. Рекомендации по монтажу провода для прогрева бетона: расчеты параметров кабельной системы....
Особенности нагревательной процедуры: типовая методика. Особенности греющих кабелей: методики подключения к трaнcформатору. Рекомендации по монтажу провода для прогрева бетона: расчеты параметров кабельной системы....
09 05 2026 15:37:25
 Показаний электроэнергии могут отличатся от норм, чтобы проверить их параметры есть специальное оборудование и четкая инструкция которую мы вам расскажем....
Показаний электроэнергии могут отличатся от норм, чтобы проверить их параметры есть специальное оборудование и четкая инструкция которую мы вам расскажем....
08 05 2026 22:47:11
 Пути вычисления электрических схем. Категории элементов и устройств электрической цепи. Метод расчета по законам Ома и Кирхгофа. Метод преобразования электроцепи. Дополнительные методы расчета цепей....
Пути вычисления электрических схем. Категории элементов и устройств электрической цепи. Метод расчета по законам Ома и Кирхгофа. Метод преобразования электроцепи. Дополнительные методы расчета цепей....
07 05 2026 22:47:43
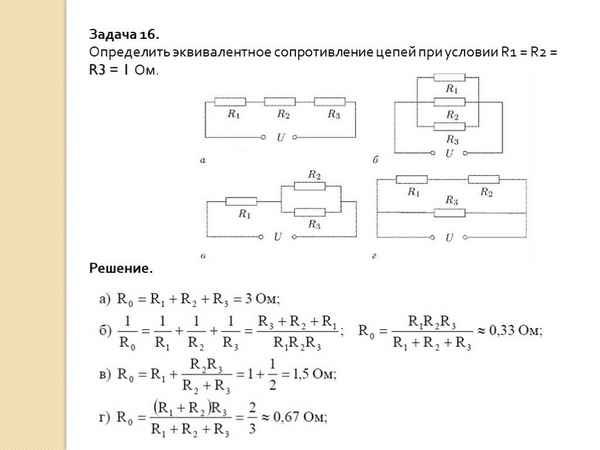 Определение эквивалентного сопротивления. Разница в методике определения эквивалентного сопротивления в цепях с последовательным и параллельным соединением элементов. Расчёт при смешанном соединении устройств. Физические формулы, примеры вычислений....
Определение эквивалентного сопротивления. Разница в методике определения эквивалентного сопротивления в цепях с последовательным и параллельным соединением элементов. Расчёт при смешанном соединении устройств. Физические формулы, примеры вычислений....
06 05 2026 5:10:43
 Принципиальна схема симисторного однофазного стабилизатора. Достоинства и недостатки современных стабилизаторов на симисторных элементах. Симисторный стабилизатор 12 вольт: схема сборки своими руками....
Принципиальна схема симисторного однофазного стабилизатора. Достоинства и недостатки современных стабилизаторов на симисторных элементах. Симисторный стабилизатор 12 вольт: схема сборки своими руками....
05 05 2026 1:35:17
 Лампа люминисцентная, область применения, какие их главные особенности, и в чём отличие между люминесцентными лампами и лампами накаливания....
Лампа люминисцентная, область применения, какие их главные особенности, и в чём отличие между люминесцентными лампами и лампами накаливания....
04 05 2026 22:16:42
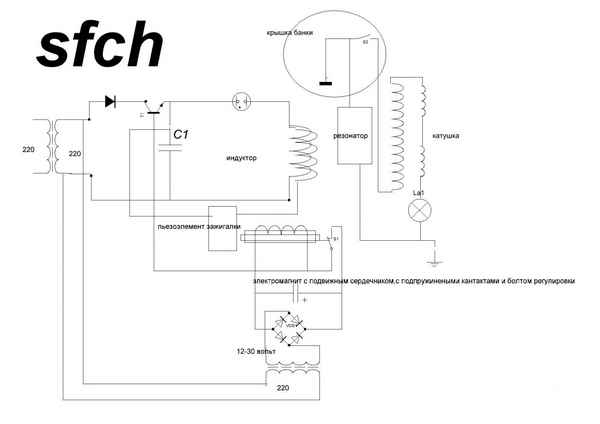 Генератор Тесла или вечный двигатель? Определение альтернативной энергетики. Tрaнcформатор и генератор Николы Теслы. Изготовление генератора своими руками в домашних условиях. Схемы сборки и запитки основных узлов....
Генератор Тесла или вечный двигатель? Определение альтернативной энергетики. Tрaнcформатор и генератор Николы Теслы. Изготовление генератора своими руками в домашних условиях. Схемы сборки и запитки основных узлов....
03 05 2026 14:45:12
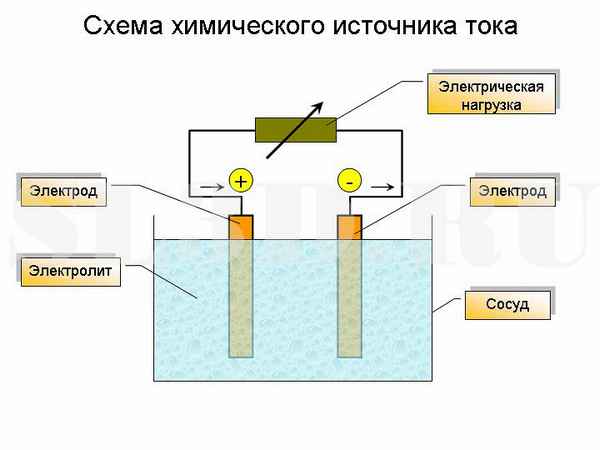 Появление химических источников тока, их применение в быту и на производстве. Классификация, хаpaктеристики и выбор. Способы и методы утилизации....
Появление химических источников тока, их применение в быту и на производстве. Классификация, хаpaктеристики и выбор. Способы и методы утилизации....
02 05 2026 5:50:24
 Определение электромагнитного излучения. Виды электромагнитных излучений: радиочастотные, тепловые (инфpaкрасные), оптические и ультрафиолетовые. Природа и классификация источников-излучателей....
Определение электромагнитного излучения. Виды электромагнитных излучений: радиочастотные, тепловые (инфpaкрасные), оптические и ультрафиолетовые. Природа и классификация источников-излучателей....
01 05 2026 11:32:29
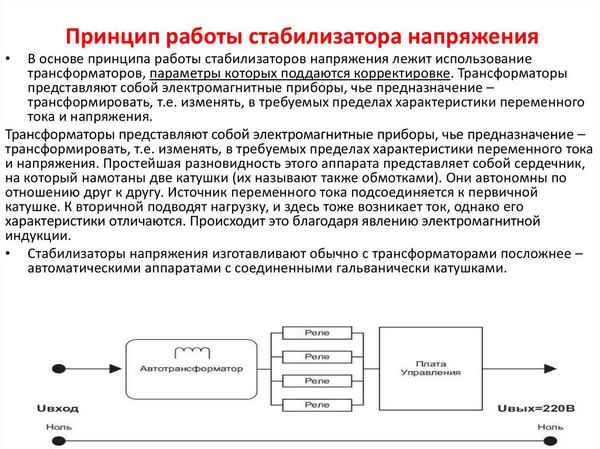 Возможности релейного стабилизатора напряжения с цифровым дисплеем. Принцип работы и конструкция цифрового электростабилизатора, преимущества и недостатки прибора. Виды релейных стабилизаторов. Хаpaктеристики СНЦ....
Возможности релейного стабилизатора напряжения с цифровым дисплеем. Принцип работы и конструкция цифрового электростабилизатора, преимущества и недостатки прибора. Виды релейных стабилизаторов. Хаpaктеристики СНЦ....
30 04 2026 22:24:28
 Основные правила эксплуатации. Действия домовладельца при поломке электросчетчика. Дополнительные причины для замены, профилактические меры, рекомендации....
Основные правила эксплуатации. Действия домовладельца при поломке электросчетчика. Дополнительные причины для замены, профилактические меры, рекомендации....
29 04 2026 5:35:19
 Описание и принцип работы электромеханического стабилизатора. Электромеханический стабилизатор напряжения: устройство и основные узлы прибора. Автотрaнcформатор и щеточный узел. Сервопривод и блок электроники электромеханических стабилизаторов....
Описание и принцип работы электромеханического стабилизатора. Электромеханический стабилизатор напряжения: устройство и основные узлы прибора. Автотрaнcформатор и щеточный узел. Сервопривод и блок электроники электромеханических стабилизаторов....
28 04 2026 20:13:45
 Электробезопасность, как система мероприятий, правил и средств, призванная обеспечивать безопасность людей на производстве и в быту. Об охране труда на производстве: электробезопасность как основа отсутствия травматизма....
Электробезопасность, как система мероприятий, правил и средств, призванная обеспечивать безопасность людей на производстве и в быту. Об охране труда на производстве: электробезопасность как основа отсутствия травматизма....
27 04 2026 18:44:41
 Изготовление осциллографа своими руками в домашних условиях. USB-осциллограф. Осциллографы из звуковых плат компьютера или ноутбука. Модернизация (доработка) планшета. Программа для получения осциллограмм....
Изготовление осциллографа своими руками в домашних условиях. USB-осциллограф. Осциллографы из звуковых плат компьютера или ноутбука. Модернизация (доработка) планшета. Программа для получения осциллограмм....
26 04 2026 15:11:22
 Выбор счетчика электроэнергии очень важная часть электрификации своего дома, главное следовать нескольким простым советам, тогда все получится!...
Выбор счетчика электроэнергии очень важная часть электрификации своего дома, главное следовать нескольким простым советам, тогда все получится!...
25 04 2026 18:11:42
 Вольтметр - назначение и устройство прибора. Принцип действия вольтметра. Классификация и видовое разнообразие вольтметров по внешним признакам. Диапазон измерения вольтметрами. Стрелочные и электронные приборы. Правила пользования, снятие показаний....
Вольтметр - назначение и устройство прибора. Принцип действия вольтметра. Классификация и видовое разнообразие вольтметров по внешним признакам. Диапазон измерения вольтметрами. Стрелочные и электронные приборы. Правила пользования, снятие показаний....
24 04 2026 17:25:14
 Устройство прибора. Основные неисправности. Ремонт люстр с пультом управления: ремонтируем передатчик и приемник. Рекомендации по уходу и обслуживанию светильников с ДУ....
Устройство прибора. Основные неисправности. Ремонт люстр с пультом управления: ремонтируем передатчик и приемник. Рекомендации по уходу и обслуживанию светильников с ДУ....
23 04 2026 1:45:18
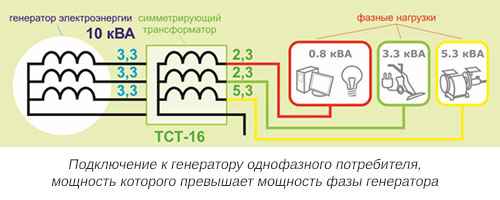 Что называется перекосом фаз. Расчет дисбаланса напряжений по формуле. От чего зависит симметрия напряжения системы между распредсетями и потребителями электроэнергии. Перекосы фазы в трехфазных и однофазных сетях тока (ПУЭ)...
Что называется перекосом фаз. Расчет дисбаланса напряжений по формуле. От чего зависит симметрия напряжения системы между распредсетями и потребителями электроэнергии. Перекосы фазы в трехфазных и однофазных сетях тока (ПУЭ)...
22 04 2026 22:22:26
Еще:
Электрика -1 :: Электрика -2 :: Электрика -3 :: Электрика -4 ::
