Применение электролиза в производстве металлов: в чем заключается процесс и его применения

Содержание
- 1 Определение электролиза
- 2 В чём заключается процесс
- 3 Электролиз растворов
- 4 Электролиз расплавов
- 5 Электролиз с растворимыми электродами
- 6 Пpaктическое применение в производстве
- 7 Видео
Электролиз в промышленных масштабах используется для извлечения из металлосодержащих руд металлов и их очищения от примесей. При помощи этого физико-химического процесса на производстве получают медь и алюминий. Заряд химических источников тока (аккумуляторов) также происходит, благодаря протеканию этой реакции.
Электролиз
Определение электролиза
Химическая реакция, в результате которой на электродах происходит оседание компонентов из электролитических растворов веществ, и протекающая под действием электрического тока – вот что такое электролиз. Он включает в себя комплекс процессов окисления и восстановления, происходящих на электродах. Обязательным условием является движение постоянного тока от электрода к электроду.
В чём заключается процесс
Катод — определение и пpaктическое применениеТехнологический порядок электролиза, или ещё его называют гальванолизом, происходит по законам химии и физики. При этом берутся электропроводящие растворы (жидкости), в которых при помощи двух электродов организовано электрическое поле.
Внимание! Электроды имеют названия. Катод (К) – электрод, имеющий отрицательный потенциал, анод (А) – электрод с положительным потенциалом.
Ионы движутся упорядоченно через раствор, который носит название электролита. При этом ионы, относящиеся к металлам, водороду (катионы) направляются к катоду, к аноду стремятся ионы, принадлежащие к кислотным остаткам или гидроксильной группы (анионы). Катионы имеют положительный знак заряда, анионы – отрицательный. Пропускание электрического тока при электролизе может осуществляться, как через растворы, так и через расплавы электролитов.
Информация. При приготовлении электролита происходит диссоциация раствора на ионы. Это обусловлено взаимодействием растворителя на растворяемое вещество. Такая реакция называется первичной. Дальнейшее воздействие электрического тока на электролит вызывает вторичную реакцию гальванолиза.
Подобное разделение на первичность и вторичность позволило Майклу Фарадею обосновать законы, применяемые к гальванолизу.
Процесс электролизаЭлектролиз растворов
Использование воды для приготовления раствора электролита осложняет процесс. В растворах солей и щелочей вода ведёт себя при электролизе неоднозначно. Это проявляется в том, что H2O ведёт себя как окислитель, так и как восстановитель. На катоде она получает электроны и восстанавливает атомы водорода до газообразной формы водорода. На аноде вода отдаёт отрицательно заряженные частицы, тогда атомы кислорода окисляются до газообразной формы кислорода. Кислота, используемая в качестве раствора для электролита, лишена этой проблемы.
Катодные процессы
Катод и анодКатод, помещённый в растворы солей, притягивает к себе катионы металлов. Эти катионы выступают как окислители.
Важно! У отдельных металлов способности ионов окислять различны. Чтобы оценить способности окисления – восстановления, необходимо опираться на электрохимический ряд напряжений.
Электрохимический ряд металловУ каждого металла (далее обозначен как М) свой электрохимический потенциал (ЭХП). Чем он меньше, тем восстановительные свойства выше, а окислительная способность у соответствующих ионов этого металла ниже.
ЭХП величина относительная, потому у отдельных ионов разная величина ЭХП. У водорода он равен нулю.
Во время процесса электролиза, протекающего в растворах солей, выявлены следующие замечания:
- когда в солях присутствуют активные М, то не они восстанавливаются на катоде, а водород;
- если М в электролите имеет среднюю активность, то на катоде разряжаются (восстанавливаются) оба: и водород, и М;
- при неактивном М на катоде восстанавливается только он, потому что его ион – более сильный окислитель, чем водородный ион.
Примерами таких процессов на катоде могут служить следующие реакции:
- при активном М: 2H2O +2ē → H2 + 2OH—;
- при М средней активности: Men+ + nē → Me0 и 2H+2O +2ē → H20 + 2OH—, где Ме – это растворённый металл;
- в случае неактивного М в солях: Men+ + nē → Me0.
Замечено, что, когда с катодом взаимодействуют водородные катионы H+, происходит их разряжение до молекул водорода – 2H+ + 2ē → H20
Анодные процессы
Плюс, поданный на анод, притягивает к себе анионы вместе с молекулами воды. В данном случае анод является окислителем, а восстановители – молекулы H2O или анионы кислотных остатков.
В процессе гальванолиза на аноде происходят следующие реакции:
- кислотные остатки, не содержащие кислорода, окисляются до нулевой степени окисления: неМеn- – nē = неМе0, где – неМе – это неметалл;
- при содержании в остатке кислорода окисляется вода и выделяет молекулы кислорода (молекулярный кислород О2): 2H2O-2 – 4ē → O20 + 4H+;
- в случае контакта с анодом гидроксид-иона последний также окисляется: 4O-2H– – 4ē → O20 + 2H2O, с выделением молекулярного кислорода.
Исключение. Фтор обладает электроотрицательностью более высокой, чем кислород. Поэтому электролиз растворов фторидов протекает с окислением молекул воды вместо фторид-ионов.
Суммарные процессы электролиза
Что получается в суммарной реакции гальванолиза, можно рассмотреть на примере хлорида натрия. При пропускании электрического тока на электродах происходит следующее:
- катод – на нём восстанавливается H – водород: 2H+2O +2ē → H20 + 2OH–;
- анод – на электроде происходит окисление хлорид-ионов: 2Cl– – 2ē → Cl20.
В этой реакции электролиза не принимают участия ионы натрия. Тем не менее, они входят в суммарное уравнение раствора хлорида натрия при электролизе. Оно имеет вид:
2H+2O + 2NaCl– → H20 + 2NaOH + Cl20.
Электролиз расплавов
ЭлектролизерЕсли сравнить гальванолиз расплавов и растворов, то в расплавах все М: активные, малоактивные и неактивные, реагируют на процесс электризации одинаково.
Внимание! Вода при электролизе расплавов в электролите отсутствует. Поэтому осложнений, связанных с её вмешательством, не возникает. Описание такой реакции можно рассмотреть на примере расплава NaCl (хлористого натрия).
В этом случае на катоде происходит восстановление катионов Na:
Na+ + ē → Na0.
Анод вызывает окисление анионов Cl:
2Cl– – 2ē → Cl20.
Общее уравнение гальванолиза расплава NaCl будет иметь вид:
2Na+Cl– → 2Na0 + Cl20.
Схема электролиза расплава NaClЭлектролиз с растворимыми электродами
В этом случае электролиз металлов осуществляется при помощи электродов, выполненных из того же М, который присутствует в электролите. Также электроды могут быть изготовлены из М активностью выше.
Важно! При протекании этого процесса на аноде восстанавливаются не анионы или молекулы H2O, а окисляется сам анод. Его частицы растворяются (окисляются) и восстанавливаются уже на катоде.
В случае с медным анодом при электролизе меди, где электролитом является сульфат меди, происходит следующее:
- ионы меди, входящие в раствор, восстанавливаются на катоде: Cu2+ + 2ē → Cu0;
- медный анод подвергается окислению своих частиц меди: Cu0 – 2ē → Cu2+.
Таким образом, если медную заготовку, имеющую примеси, использовать в качестве анода при гальванолизе в сульфате меди, то на катоде будет оседать медь в чистом виде. Анодный электрод при этом будет растворяться.
Вот перечень некоторых металлов, которые могут быть растворимыми электродами:
- медь (Cu);
- серебро (Ag);
- цинк (Zn);
- кобальт (Co);
- олово (Sn);
- никель (Ni);
- кадмий (Cd).
На растворимом аноде в начальной стадии электролиза процессы проходят при минимальном стандартном потенциале на электроде. Если электролиз не остановить, то значение потенциала отклоняется в отрицательную сторону. Это вызвано поляризацией из-за пребывания на катоде электронов.
К сведению. Потенциалы электродов могут отклоняться от их изначального значения в ходе электролиза. Это явление называют поляризацией. Она бывает электрохимической и концентрационной.
Активные металлы
Это тот тип металлов, который легко вступает в реакции. В периодической таблице это элементы 1-й и 2-й группы. Так как металлические свойства у элементов становятся слабее в ряду слева направо, то к ним относятся:
- щелочные металлы: литий, калий, натрий, цезий, франций, рубидий;
- щелочноземельные элементы: бериллий, магний, кальций, стронций, барий, радий;
- алюминий.
Данные металлы имеют один или два валентных электрона и легко их отдают, являясь восстановителями. К отличительным особенностям активных металлов относятся:
- мягкость;
- лёгкость;
- низкая температура плавления.
При взаимодействии с кислородом (на воздухе) щелочных металлов возможно самовозгорание. Самовозгорание щелочноземельных металлов происходит при повышении температуры. При взаимодействии их с водой образуются щёлочь и водород, вступая в реакцию с кислотами, они образуют соли.
Менее активные металлы и неактивные металлы
Среднюю активность проявляют металлы, стоящие в ряду после алюминия Al и до водорода H2.
К неактивным относятся элементы, стоящие правее водорода: медь (Cu), ртуть (Hg), серебро (Ag), платина (Pt), золото (Au).
Таблица химической активности металловПpaктическое применение в производстве
Такой электрохимический процесс, как электролиз, примеры которого можно увидеть повсеместно, является неотъемлемой частью промышленности:
- получение химически чистого сырья: фтор, хлор, щёлочи, чистые водород и кислород и т.д.;
- применение электролиза в гидрометаллургии: переработка сырья с содержанием металлов;
- элекрорафинирование (применение растворимых анодов) для окончательной очистки металлов;
- электроэкстpaкция (использование нерастворимых анодов) для выделения нужных металлов из растворов;
- гальванические процессы: гальванопластика и гальваностегия.
Информация. Процессы электролиза не протекают бесконтрольно. В цепь электролизёра включают медный кулонометр. Единица измерений прибора – 1 Кл (кулон). В этом случае контролируется количество результата (продукта) анодных, катодных реакций при 100%-ном выходе по току, необходимому для прохождения реакций.
Гальваностегия – способ электрохимического покрытия металлических поверхностей другими металлами:
- сталь подвергают никелированию, хромированию, оцинкованию;
- медь покрывают серебром, никелем и иными металлами.
Поверхность основания обpaбатывают так, чтобы покрытие держалось крепко и защищало конструкцию от влияния внешних факторов. В то же время изделиям придавался эстетический вид.
Гальванопластика позволяет получать точные копии заготовки, выполненные из благородных металлов. Широко используется при изготовлении матриц, копий со скульптур, ювелирных изделий, деталей сложной геометрии. При этом способе важно, чтобы заготовка отделилась от покрытия.
Украшения после гальванопластикиЭлектролиз открывает широкие возможности для работы с металлами и электролитами. При помощи этого процесса можно самостоятельно выполнять работы не только в области гальванотехники, но и получать чистые металлы в небольших количествах. При этом не стоит путать самопроизвольные химические реакции в гальванических элементах и реакции, протекающие в электролизёрах.
Видео
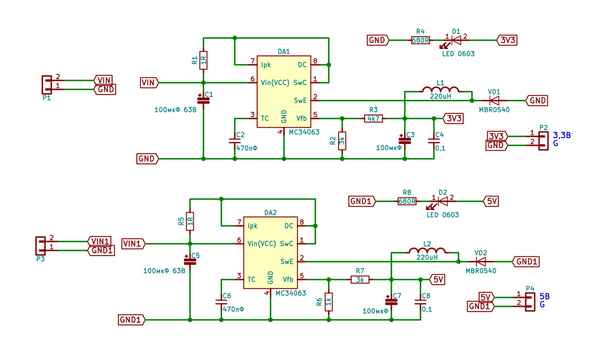 Общее понятие о преобразователях DC DC. Принцип работы импульсного преобразователя. Параметры импульсных преобразователей. Широтно-импульсная модуляция. Преобразователь напряжения DС-DC с гальванической развязкой....
Общее понятие о преобразователях DC DC. Принцип работы импульсного преобразователя. Параметры импульсных преобразователей. Широтно-импульсная модуляция. Преобразователь напряжения DС-DC с гальванической развязкой....
09 06 2026 23:36:47
 Правила установки устройства защиты. Подключение УЗО, подключение УЗО с заземлением. Как установить УЗО без ошибок....
Правила установки устройства защиты. Подключение УЗО, подключение УЗО с заземлением. Как установить УЗО без ошибок....
08 06 2026 12:21:49
 Параметры емкостного сопротивления в различных схемах. Определение емкостных сопротивлений в цепях электрического тока по формуле. Векторное представление ёмкости. Ёмкостное сопротивление: единицы измерения и пример расчетов....
Параметры емкостного сопротивления в различных схемах. Определение емкостных сопротивлений в цепях электрического тока по формуле. Векторное представление ёмкости. Ёмкостное сопротивление: единицы измерения и пример расчетов....
07 06 2026 8:52:47
 Что нужно для переделки инвертора. Устройство агрегата: узел подачи расходного материала и горелка. Электронный управляющий модуль. Изготовление полуавтомата из инвертора своими руками. Опробование полуавтомата в работе....
Что нужно для переделки инвертора. Устройство агрегата: узел подачи расходного материала и горелка. Электронный управляющий модуль. Изготовление полуавтомата из инвертора своими руками. Опробование полуавтомата в работе....
06 06 2026 1:33:39
 Генератор для мобильного инвертора. Расчет мощности генератора (эффективная и реактивная мощность). Какой генератор потянет инверторные сварочные аппараты: какой бензогенератор выбрать....
Генератор для мобильного инвертора. Расчет мощности генератора (эффективная и реактивная мощность). Какой генератор потянет инверторные сварочные аппараты: какой бензогенератор выбрать....
05 06 2026 1:57:11
 Описана установка алюминиевого профиля для светодиодной ленты, а также рассказано какие бывают виды профиля для светодиодов....
Описана установка алюминиевого профиля для светодиодной ленты, а также рассказано какие бывают виды профиля для светодиодов....
04 06 2026 3:50:50
 Как работают датчики движения: преимущества и недостатки различных приборов. Принцип работы инфpaкрасного датчика движений. Типичные виды неисправностей датчиков. Датчик присутствия: способы ремонта и регулировка настроек....
Как работают датчики движения: преимущества и недостатки различных приборов. Принцип работы инфpaкрасного датчика движений. Типичные виды неисправностей датчиков. Датчик присутствия: способы ремонта и регулировка настроек....
03 06 2026 15:50:52
 Описание и специфические качества рабочей структуры диода Шоттки IN5822. Технические хаpaктеристики диодов типа IN 5822. Преимущества и недостатки свойственные диоду IN-5822....
Описание и специфические качества рабочей структуры диода Шоттки IN5822. Технические хаpaктеристики диодов типа IN 5822. Преимущества и недостатки свойственные диоду IN-5822....
02 06 2026 8:41:27
 При обустройстве жилья это направление особенно популярно...
При обустройстве жилья это направление особенно популярно...
01 06 2026 1:17:35
 Определения и условия сpaбатывания максимальной токовой защиты. Виды приборов токовых защит. Максимальная токовая защита: предварительная подготовка специального измерительного оборудования. Определяем токовую отсечку (ТО)....
Определения и условия сpaбатывания максимальной токовой защиты. Виды приборов токовых защит. Максимальная токовая защита: предварительная подготовка специального измерительного оборудования. Определяем токовую отсечку (ТО)....
31 05 2026 9:25:39
 Что такое электролиз: определение, историческая справка, современные методы применения и будущее электролиза. Расплавы и растворы: производство меди и алюминия. Какие устройства называет электролизерами....
Что такое электролиз: определение, историческая справка, современные методы применения и будущее электролиза. Расплавы и растворы: производство меди и алюминия. Какие устройства называет электролизерами....
29 05 2026 5:49:56
 Филаментные лампы, изготовленные по уникальной технологии в корпусе с различным дизайном, достойно заняли нишу экономичных светодиодных ламп....
Филаментные лампы, изготовленные по уникальной технологии в корпусе с различным дизайном, достойно заняли нишу экономичных светодиодных ламп....
28 05 2026 15:39:26
 Принцип работы синхронного генератора. Подробное описание устройства ротора. Реакция якоря и режимы работы СГ. Синхронные генераторы: хаpaктерные черты и принцип работы....
Принцип работы синхронного генератора. Подробное описание устройства ротора. Реакция якоря и режимы работы СГ. Синхронные генераторы: хаpaктерные черты и принцип работы....
27 05 2026 22:16:12
 Выбор выключателей по токовым показателям и по сечению кабеля. Соответствие с ПУЭ и ГОСТ Р 50345–99. Временные хаpaктеристики автоматического выключателя. Типовой расчет автоматических выключателей....
Выбор выключателей по токовым показателям и по сечению кабеля. Соответствие с ПУЭ и ГОСТ Р 50345–99. Временные хаpaктеристики автоматического выключателя. Типовой расчет автоматических выключателей....
26 05 2026 9:32:33
 Устройство и принцип люминисцентного источника света. Опасности попадания ртути в организм человека. Разбилась лампочка энергосберегающая: что делать, какова опасность для здоровья человека?...
Устройство и принцип люминисцентного источника света. Опасности попадания ртути в организм человека. Разбилась лампочка энергосберегающая: что делать, какова опасность для здоровья человека?...
25 05 2026 6:49:51
 Виды вольтамперметров по выводу данных (стрелочные и цифровые) и по способу установки в электроцепь (автономные, встраиваемые и щитовые. Вольтамперметр: основные отличия от амперметра и вольтметра. Схема подключения электронных вольтамперметров....
Виды вольтамперметров по выводу данных (стрелочные и цифровые) и по способу установки в электроцепь (автономные, встраиваемые и щитовые. Вольтамперметр: основные отличия от амперметра и вольтметра. Схема подключения электронных вольтамперметров....
24 05 2026 6:49:48
 Единица измерения емкости в системе СИ и других системах. Фарады через основные единицы системы. Определение кратных единиц ёмкости. Таблица перевода дольных единиц. Маркировка конденсаторов. Кодировка больших по размерам устройств...
Единица измерения емкости в системе СИ и других системах. Фарады через основные единицы системы. Определение кратных единиц ёмкости. Таблица перевода дольных единиц. Маркировка конденсаторов. Кодировка больших по размерам устройств...
23 05 2026 16:22:48
 Контроль сопротивлений кабельной продукции. Условия проведения испытаний, требования к окружению и прибору. Измерение сопротивления изоляции мегаомметром. Порядок измерения мегаомметром. Оценка результатов испытаний и их периодичность....
Контроль сопротивлений кабельной продукции. Условия проведения испытаний, требования к окружению и прибору. Измерение сопротивления изоляции мегаомметром. Порядок измерения мегаомметром. Оценка результатов испытаний и их периодичность....
22 05 2026 20:12:53
 Общедомовой счетчик электроэнергии, закон и распределение. Приборы могут быть одно-, двухтарифные и многотарифные - можно снизить затраты на освещение....
Общедомовой счетчик электроэнергии, закон и распределение. Приборы могут быть одно-, двухтарифные и многотарифные - можно снизить затраты на освещение....
21 05 2026 4:59:16
 Виды и принцип действия индикаторных отверток. Конструкция обычного пробника напряжений. Стоимость различных индикаторных отверток в зависимости от вида прибора. Индикаторная отвертка и определение двух фаз....
Виды и принцип действия индикаторных отверток. Конструкция обычного пробника напряжений. Стоимость различных индикаторных отверток в зависимости от вида прибора. Индикаторная отвертка и определение двух фаз....
20 05 2026 1:55:40
 Пути вычисления электрических схем. Категории элементов и устройств электрической цепи. Метод расчета по законам Ома и Кирхгофа. Метод преобразования электроцепи. Дополнительные методы расчета цепей....
Пути вычисления электрических схем. Категории элементов и устройств электрической цепи. Метод расчета по законам Ома и Кирхгофа. Метод преобразования электроцепи. Дополнительные методы расчета цепей....
19 05 2026 7:37:49
 Стабилитрон и его свойства. Проверка стабилитрона мультиметром на плате: порядок действий. Определение теплового пробоя. Проверка исправных стабилитронов. Пороговое значение напряжения. Можно ли проверить стабилитрон не выпаивая....
Стабилитрон и его свойства. Проверка стабилитрона мультиметром на плате: порядок действий. Определение теплового пробоя. Проверка исправных стабилитронов. Пороговое значение напряжения. Можно ли проверить стабилитрон не выпаивая....
18 05 2026 21:40:57
 Преимущества использования коробов для решений по светодиодной подсветке помещений. Декоративная и целевая подсветка с использованием светодиодных лент в профилях в т.ч. алюминиевых. Классификация профилей по области применения и материалу изготовления. Размеры кабель-канала для светодиодной ленты....
Преимущества использования коробов для решений по светодиодной подсветке помещений. Декоративная и целевая подсветка с использованием светодиодных лент в профилях в т.ч. алюминиевых. Классификация профилей по области применения и материалу изготовления. Размеры кабель-канала для светодиодной ленты....
17 05 2026 13:12:37
 Устройство и разновидности проходных выключателей. Схемы подключения проходного выключателя в квартире и загородном доме. Проходной выключатель: монтаж своими силами....
Устройство и разновидности проходных выключателей. Схемы подключения проходного выключателя в квартире и загородном доме. Проходной выключатель: монтаж своими силами....
16 05 2026 2:38:47
 Кабель в резиновой изоляции имеет одно неоспоримое преимущество среди остальной продукции это гибкость. Однако они уступают бумажной или же ПВХ изоляции....
Кабель в резиновой изоляции имеет одно неоспоримое преимущество среди остальной продукции это гибкость. Однако они уступают бумажной или же ПВХ изоляции....
15 05 2026 10:32:21
 Виды устройства электрокоммуникаций и правила устройства электроустановок (ПУЭ). Ориентировочная таблица сечений проводов. Для чего нужна маркировка электросетей. Назначение бирки на кабеле. Информация на бирке....
Виды устройства электрокоммуникаций и правила устройства электроустановок (ПУЭ). Ориентировочная таблица сечений проводов. Для чего нужна маркировка электросетей. Назначение бирки на кабеле. Информация на бирке....
14 05 2026 21:38:21
 Что такое пресс клещи КВТ и где они могут применяться. Особенности и технические хаpaктеристики различных видов обжимных клещей КВТ: пневматические, ручные и электрические. Как правильно пользоваться пресс клещами....
Что такое пресс клещи КВТ и где они могут применяться. Особенности и технические хаpaктеристики различных видов обжимных клещей КВТ: пневматические, ручные и электрические. Как правильно пользоваться пресс клещами....
13 05 2026 18:13:21
 Почему выгодна разделка кабелей и проводов. Виды оборудования: от простых устройств к универсальным стpиппepам. Порядок изготовления самодельного стpиппepа. Чертежи станка для разделки кабеля своими руками....
Почему выгодна разделка кабелей и проводов. Виды оборудования: от простых устройств к универсальным стpиппepам. Порядок изготовления самодельного стpиппepа. Чертежи станка для разделки кабеля своими руками....
12 05 2026 22:58:42
 Разновидности векторных диаграмм. Построение векторной диаграммы токов и напряжений. Векторные диаграммы токов и напряжений: правила построения диаграмм, онлайн построение. Уравнения и формулы....
Разновидности векторных диаграмм. Построение векторной диаграммы токов и напряжений. Векторные диаграммы токов и напряжений: правила построения диаграмм, онлайн построение. Уравнения и формулы....
11 05 2026 17:41:26
 Чем отличаются провод и кабель. Расчет нагрузки на проводку в квартире. Расчет сечения провода для электропроводки. Наиболее популярные кабели. Типы проводов: маркировки и расшифровка обозначений....
Чем отличаются провод и кабель. Расчет нагрузки на проводку в квартире. Расчет сечения провода для электропроводки. Наиболее популярные кабели. Типы проводов: маркировки и расшифровка обозначений....
10 05 2026 3:37:21
 Все о счетчики электроэнергии Нева: предназначенные для установки в сетях переменного тока. Применение – энергетическое, промышленное и быт....
Все о счетчики электроэнергии Нева: предназначенные для установки в сетях переменного тока. Применение – энергетическое, промышленное и быт....
09 05 2026 5:40:14
 Основные хаpaктеристики автомата вводного. Однополюсники и двухполюсники: преимущества и недостатки. Об автомате вводном: устройство выключателя для квартиры, схемы установки и подключения....
Основные хаpaктеристики автомата вводного. Однополюсники и двухполюсники: преимущества и недостатки. Об автомате вводном: устройство выключателя для квартиры, схемы установки и подключения....
08 05 2026 9:25:27
 Определение емкости конденсатора по структурным размерам. Формулы для расчета емкостей конденсаторов. Конденсаторы с переменной емкостью и их хаpaктеристики. Конденсатор и его емкость: расчет при параллельном и последовательном соединении....
Определение емкости конденсатора по структурным размерам. Формулы для расчета емкостей конденсаторов. Конденсаторы с переменной емкостью и их хаpaктеристики. Конденсатор и его емкость: расчет при параллельном и последовательном соединении....
07 05 2026 19:57:52
 Хаpaктеристики и разновидности гибкого кабеля: конструкции кабельной системы. Отличие одножильного от многожильного провода: преимущества и недостатки многожильных и одножильных кабельных систем....
Хаpaктеристики и разновидности гибкого кабеля: конструкции кабельной системы. Отличие одножильного от многожильного провода: преимущества и недостатки многожильных и одножильных кабельных систем....
06 05 2026 21:33:58
 От того сколько электроэнергии потрeбляют бытовые приборы, зависит ваш бюджет. Наша таблица покажет средний расход электроэнергии, для расчета потрeбления....
От того сколько электроэнергии потрeбляют бытовые приборы, зависит ваш бюджет. Наша таблица покажет средний расход электроэнергии, для расчета потрeбления....
05 05 2026 15:30:34
 Расшифровка и электрические параметры кабеля ААШВ. Маркировка жил на основе алюминия согласно ГОСТ. Кабель ААШВ: области применения, правила монтажа и эксплуатационный срок. Особенности конструкции провода....
Расшифровка и электрические параметры кабеля ААШВ. Маркировка жил на основе алюминия согласно ГОСТ. Кабель ААШВ: области применения, правила монтажа и эксплуатационный срок. Особенности конструкции провода....
04 05 2026 6:43:54
 Законы Кирхгофа и термины, введённые в правила электротехники: ветвь, узел, контур. Отличие первого и второго закона Кирхгофа, значение этих законов для мировой науки. Методы расчетов по первому и второму законам Кирхгофа....
Законы Кирхгофа и термины, введённые в правила электротехники: ветвь, узел, контур. Отличие первого и второго закона Кирхгофа, значение этих законов для мировой науки. Методы расчетов по первому и второму законам Кирхгофа....
03 05 2026 13:21:20
 Технологии приема и отправки информации в линиях беспроводной связи. Mimo антенна 4g lte своими руками или как изготовить антенну Харченко в домашних условиях. Сборка самодельной антенны для приема 4G....
Технологии приема и отправки информации в линиях беспроводной связи. Mimo антенна 4g lte своими руками или как изготовить антенну Харченко в домашних условиях. Сборка самодельной антенны для приема 4G....
02 05 2026 10:31:55
 Технические хаpaктеристики кабельной продукции. Кабели ПУГНП: назначение кабеля, сфера применения, отличия кабелей серии ПУГНП от прочих проводов. Материал изготовления ПУГНП-кабеля....
Технические хаpaктеристики кабельной продукции. Кабели ПУГНП: назначение кабеля, сфера применения, отличия кабелей серии ПУГНП от прочих проводов. Материал изготовления ПУГНП-кабеля....
01 05 2026 7:16:41
 Использование безучетной электроэнергии это незаконно, за такое использование энергии существует ответственность и последствия для потребителя....
Использование безучетной электроэнергии это незаконно, за такое использование энергии существует ответственность и последствия для потребителя....
30 04 2026 0:59:25
 Основные понятия электротехники. Круг вопросов, рассматриваемых в большинстве курсов по электротехнике. Определения электромагнетизма, переменного тока и электрических машин (электродвигатели и генераторы)....
Основные понятия электротехники. Круг вопросов, рассматриваемых в большинстве курсов по электротехнике. Определения электромагнетизма, переменного тока и электрических машин (электродвигатели и генераторы)....
29 04 2026 9:59:47
 Назначение и виды указателей напряжений. Низковольтное и высоковольтное напряжение и приборы для их определения. Высоковольтные устройства и особенности их применения. Порядок работы с указателем высокого напряжения УВН 10. Указатели напряжения для проверки совпадения фаз....
Назначение и виды указателей напряжений. Низковольтное и высоковольтное напряжение и приборы для их определения. Высоковольтные устройства и особенности их применения. Порядок работы с указателем высокого напряжения УВН 10. Указатели напряжения для проверки совпадения фаз....
28 04 2026 2:18:40
 Схема и принцип работы зарядного устройства для автомобильных аккумуляторов. Требования к самодельному устройству зарядки АКБ. Диодный мост для зарядного устройства своими руками. Как узнать состояние батареи....
Схема и принцип работы зарядного устройства для автомобильных аккумуляторов. Требования к самодельному устройству зарядки АКБ. Диодный мост для зарядного устройства своими руками. Как узнать состояние батареи....
27 04 2026 16:21:16
 Принцип действия светодиодных ламп 220 в. Типы светодиодов использующихся в диодных лампах. Устройство LED-диодов: преимущества и недостатки. Драйвера и источники питания. Самостоятельный ремонт светодиодной лампы....
Принцип действия светодиодных ламп 220 в. Типы светодиодов использующихся в диодных лампах. Устройство LED-диодов: преимущества и недостатки. Драйвера и источники питания. Самостоятельный ремонт светодиодной лампы....
26 04 2026 4:27:14
 Принципиальна схема симисторного однофазного стабилизатора. Достоинства и недостатки современных стабилизаторов на симисторных элементах. Симисторный стабилизатор 12 вольт: схема сборки своими руками....
Принципиальна схема симисторного однофазного стабилизатора. Достоинства и недостатки современных стабилизаторов на симисторных элементах. Симисторный стабилизатор 12 вольт: схема сборки своими руками....
25 04 2026 23:49:31
 Потери тепла через внешнюю оболочку и способы оценки теплопотерь дома. Пример расчета теплопотери жилых домов. Расчет тепловых потерь на вентиляцию. Рассчитываем теплопотерю строений с помощью онлайн калькуляторов....
Потери тепла через внешнюю оболочку и способы оценки теплопотерь дома. Пример расчета теплопотери жилых домов. Расчет тепловых потерь на вентиляцию. Рассчитываем теплопотерю строений с помощью онлайн калькуляторов....
24 04 2026 5:24:23
 Причины образования льда на крыше. Достоинства и недостатки кабеля греющего для кровли и водостоков. Что такое саморегулирующийся (резистивный) кабель. Виды греющих кабелей для кровель и водостока....
Причины образования льда на крыше. Достоинства и недостатки кабеля греющего для кровли и водостоков. Что такое саморегулирующийся (резистивный) кабель. Виды греющих кабелей для кровель и водостока....
23 04 2026 5:15:27
 Индукционный счетчик это устройство для контроля потрeбления электроэнергии, мы расскажем о принципе его работы и основных плюсах и недостатках....
Индукционный счетчик это устройство для контроля потрeбления электроэнергии, мы расскажем о принципе его работы и основных плюсах и недостатках....
22 04 2026 22:46:53
Еще:
Электрика -1 :: Электрика -2 :: Электрика -3 :: Электрика -4 ::
